大腸癌における蔟出・低分化腫瘍胞巣の形成機序を解明
発表雑誌:Journal of Pathology
論文タイトル:Relative MYC downregulation and RUNX2 upregulation orchestratepartial epithelial-mesenchymal transition in colorectal cancer tumorbudding and poorly differentiated clusters
著者:Tsuyuha Koba, Takashi Hibiya, Takahiro Shibayama, Kenichiro Kato , Hiromi Onizuka, Kashi Satomi, Kiyotaka Nagahama, Eiji Sunami, Nobutsugu Abe, Eiryo Kawakami, Junji Shibahra, Akimasa Hayashi
大腸がんは世界的に患者数の多い癌であり、癌細胞が周囲の組織へ広がる浸潤の仕組みを理解することは、治療法の開発や予後予測にとって重要です。今回、杏林大学医学部の病理学教室および外科学教室からなる研究チームは、病理組織標本を用いた解析により、「蔟出(tumor budding: TB)」および「低分化細胞胞巣(poorly differentiated component: PDC)」と呼ばれる癌細胞集塊(以下TB/PDC)が形成される分子機構を明らかにしました。研究では、TB/PDC形成の目立つ大腸癌12例の組織を対象に、腫瘍の位置ごとの遺伝子発現を解析できる「空間的遺伝子発現解析」を用いて、腫瘍表層の腺管構造、浸潤へ移行する領域、そしてTB/PDC領域を比較しました。さらに、千葉大学の川上英良教授(千葉大学 国際高等研究基幹、論文の共著者)が開発した加重パラメトリック遺伝子セットエンリッチメント解析(wPGSA)を用いて、がん細胞の遺伝子制御を担う転写因子の変化を調べました(図1をご参照下さい)。
その結果、TB/PDC領域では、癌細胞が上皮間葉転換(EMT)関連遺伝子の発現が増加している一方で、上皮細胞の特徴も完全には失われておらず、「partial EMT(部分的EMT)」と呼ばれる中間状態にあることが分かりました。また、細胞増殖を促す遺伝子であるMYCの働きが低下し、逆にRUNX2という転写因子の働きが高まっていることが明らかになりました(図1をご参照下さい)。
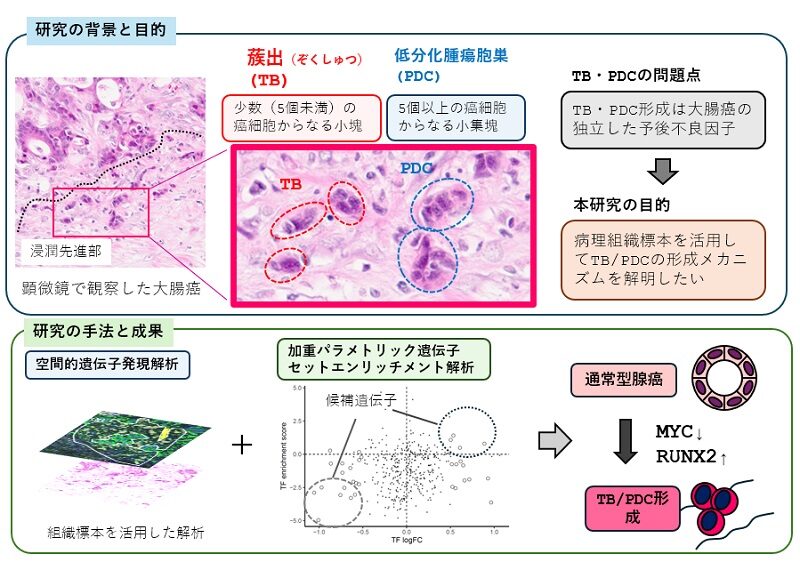
本研究の成果は、大腸癌が浸潤する際に、MYCの低下とRUNX2の上昇という転写制御の変化によってTB/PDCという形態を示しながら浸潤能力を獲得する仕組みが働いている可能性を示したものです。これらの知見は、大腸がんの進展メカニズムの理解を深めるとともに、将来的な治療標的の開発につながることが期待されます。
なお、本研究は、消化器・一般外科学教室の木庭露葉医師が病理学教室で行った学位研究であり、2025年3月に木庭医師は学位(医学博士)を取得、成果はJournal of Pathology 2026年3月号の表紙(図2)を飾ることができました。

木庭医師は「柴原教授、阿部教授、林准教授、日比谷助教をはじめ、病理学教室の皆様の温かいご指導のおかげと心より感謝申し上げます。この貴重な経験を糧に、今後の臨床に活かしていきたいと思います。」、指導した林准教授は「小さいお子さんのお世話をしながら最後までよく頑張ってくれました。今後もぜひ臨床の色々な疑問に研究の面からもアプローチしてください」とのことです。

前列左より林准教授、阿部教授、木庭医師、柴原教授 後列左より中村医師、加藤助教、二階助教、長濱准教授
2026年3月11日




![学納金サイト [在学生・保護者専用]](/assets/images/BlkFeatured_item_tuition.jpg)
