School of Medicine家族性筋萎縮性側索硬化症(ALS)の新たな原因遺伝⼦変異を発⾒― SOD1遺伝⼦の新規変異が⽰す病態理解と個別化医療への可能性
市川 弥⽣子(脳神経内科学・教授)
研究のハイライト
- ⽇本⼈の家族性ALSの1家系から、SOD1遺伝⼦の新たな変異を発⾒しました。
- この変異は世界的にも極めてまれな「インフレーム重複型」のSOD1遺伝⼦変異です。
- SOD1タンパク質の三次元(3D)構造予測からは,本変異によって構造変化が⽣じる可能性が⽰されました。
- 遺伝形式、神経病理および遺伝⼦発現解析の両⾯から、病原性機能獲得(gain of function)によるALS発症機序が⽰唆されました。
- ALSの個別化医療、遺伝⼦治療薬開発への貢献が期待される研究成果です。
概要
筋萎縮性側索硬化症(ALS)は、運動ニューロンの障害により⼿⾜やのどの筋⾁が徐々にやせていく進⾏性の神経難病です。ALSの約 5-10%は遺伝が関与する家族性ALSです。なかでも⽇本⼈では、SOD1遺伝⼦の変異により発症する「SOD1関連ALS」が最も多く、その 多くは両親のいずれかから変異を受け継ぐ常染⾊体顕性(優性)遺伝形式をとります。 杏林⼤学医学部脳神経内科学教室では、東京⼤学・⼤阪医科薬科⼤学・愛知医科⼤学・滋賀医科⼤学との共同研究で、常染⾊体顕性(優 性)遺伝形式をとる家族性ALSの⽇本⼈1家系において、SOD1遺伝⼦の「インフレーム重複」型の新しい変異(インフレーム重複変異: p.Val120dup)を同定し、その病的意義を明らかにしました。インフレーム重複変異は、遺伝⼦の読み枠を保ったままタンパク配列の⼀ 部が重複するという特殊なタイプの変異です。SOD1遺伝⼦におけるインフレーム重複変異は、ALSではこれまでに2家系しか報告されて おらず、世界的にも極めてまれなものです。 本研究成果は、SOD1遺伝⼦変異の多様性とALSの発症メカニズムの理解を深めるとともに、遺伝⼦変異に基づくALSの個別化医療や、 将来的な遺伝⼦治療薬の開発に貢献することが期待されます。
1.SOD1遺伝⼦の新しい変異(インフレーム重複変異)
本研究では、SOD1遺伝⼦解析を⾏い、新しい変異(インフレーム重複変異:p.Val120dup)を同定し、家族性ALSの原因解明に新たな知 ⾒を加えました。本変異は、遺伝⼦の読み枠を保ったまま、SOD1タンパク質の120番目のアミノ酸であるバリン(Val)が重複するとい う特殊な変異です。その結果、本来121番目に位置しているヒスチジン(H121)は122番目(H122)へとずれることが予測されます。 (図A)。 SOD1タンパク質は、体内で⽣じる有害な活性酸素を分解する酵素であり、その機能には銅イオンが活性中⼼に正しく結合することが不 可⽋です。特に121番目のヒスチジン(H121)は、銅イオンを安定して結合させるために重要な役割を担っています。したがって、本変 異によるアミノ酸配列のわずかな変化であっても、SOD1タンパク質の⽴体構造や機能に⼤きな影響を及ぼす可能性があります。
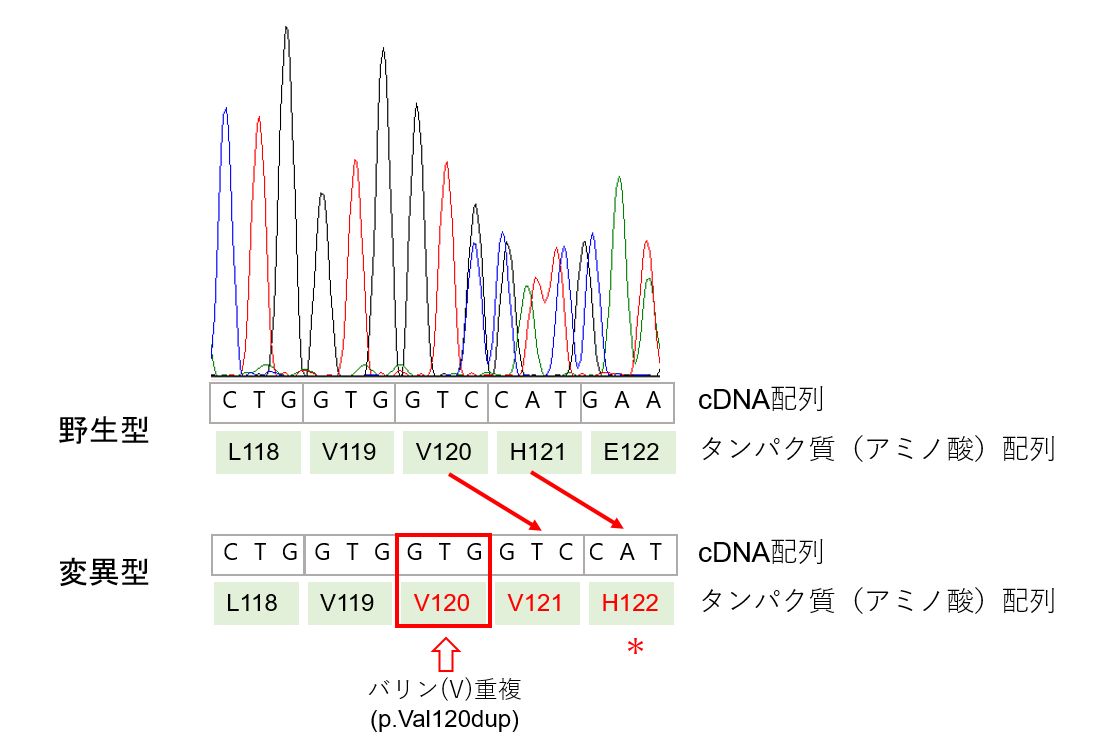
図に⽰した波形は、発症者のSOD1遺伝⼦cDNA配列の解析結果を⽰しています。変異型ではcDNA配列の⼀部に「GTG」の重複が認めら れ、読み枠は保たれたまま、SOD1タンパク質の120番目にバリン(Val)が1つ挿⼊されます(インフレーム重複)。その結果、本来121 番目に位置するヒスチジン(His)は122番目へとずれています(*)。
2.SOD1タンパク質の三次元(3D)構造変化の予測
SOD1タンパク質に⽣じる構造変化を検討するため、三次元(3D)構造解析の予測(in silico解析)を⾏いました。その結果、本変異に よって新たに⽣じたヒスチジン(H122)は、銅イオン(Cu²⁺)の結合部位から離れた場所に位置することが予測されました(図B)。こ のことから、SOD1の活性中⼼において、銅イオンが適切に結合できなくなる構造変化が⽣じる可能性が明らかになりました。 銅イオンは、SOD1の酵素活性の中⼼として機能するだけでなく、タンパク質全体の⽴体構造を安定化させる重要な役割も担っていま す。したがって、本変異により銅イオン結合が障害されることで、SOD1タンパク質が正しい⽴体構造を形成できず、異常な形になる 「ミスフォールディング(正しい形に折りたためない状態)」が引き起こされる可能性が⽰唆されました。
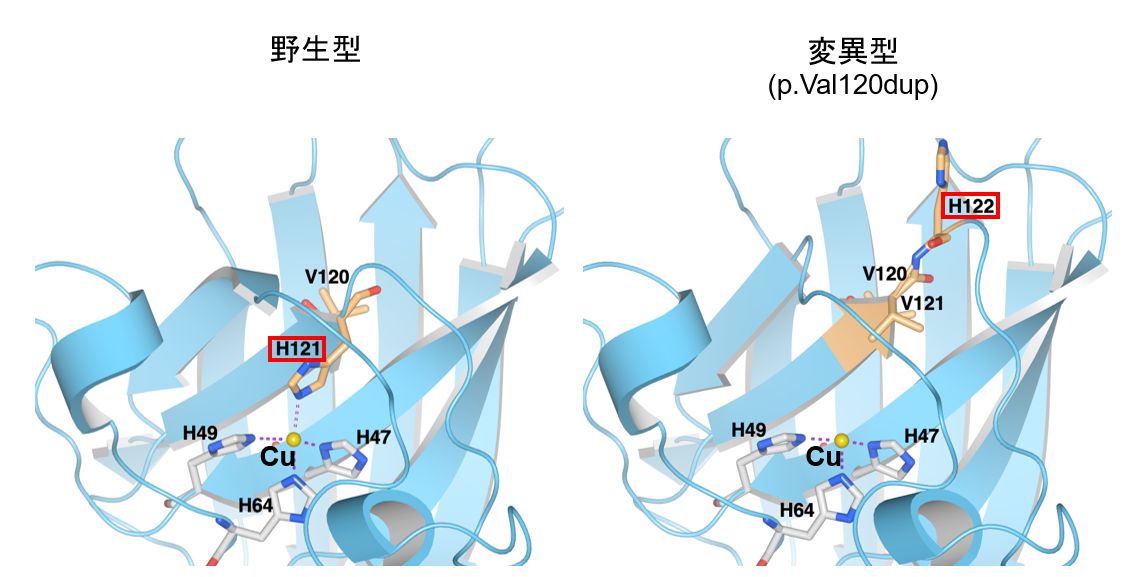
SOD1が正常に働くためには、活性中⼼に銅イオン(Cu²⁺)が結合する必要があります。図中では、銅イオンを⻩⾊の球で⽰しています。野⽣型では、4つのヒスチジン(H47、H49、H64、H121)が銅イオンを取り囲むように配置され、銅イオンをしっかりと結合します。⼀⽅、変異型SOD1では、タンパク質配列のずれによって本来121番目にあったヒスチジンが122番目(H122)に変化します。この新たに⽣じたH122は、銅イオンから離れた場所に位置するため、SOD1の活性中⼼に銅イオンが結合できなくなるという構造変化が⽣じると予測されます。
3.病原性機能獲得(gain of function)によるALS発症機序の検証
実際、神経病理学的解析において、ミスフォールディング状態のタンパク質を特異的に検出できる抗体を⽤いた免疫染⾊により、本家系
発症者の神経細胞内に異常なSOD1の凝集体が存在することを確認しました。これは、今回同定した変異(p.Val120dup)がSOD1タンパ
ク質のミスフォールディングを引き起こし、ALSの病態形成に直接関与していることを⽰す重要な証拠です。
さらに、デジタルPCRによる解析では、SOD1メッセンジャーRNAの発現量には発症者と健常対照者で変化がないことも確認されまし
た。これに加えて、SOD1関連ALSが⽚親のみから遺伝⼦変異を受け継ぐことで発症する常染⾊体顕性(優性)遺伝形式であることを踏
まえると、今回のp.Val120dup変異型SOD1は、発現量の変化によってALSを引き起こすのではなく、病気を引き起こす機能を新たに獲得
すること(gain of function)でALSの発症に⾄ることが⽰されました。
4.ALSの新規治療薬トフェルセンと個別化医療
SOD1関連ALSでは、SOD1の発現を抑制するアンチセンス核酸治療薬「トフェルセン」が、⽇本でも約1年前に承認され、実際の治療に ⽤いられるようになりました。トフェルセンは、SOD1遺伝⼦から作られるSOD1タンパク質(変異型を含む)の量を減らすことで、神 経細胞の変性を遅らせることを目的とした薬です。本研究で明らかになった、SOD1の構造変化や、新たな病原性機能の獲得(gain of function)といった病態メカニズムは、トフェルセン治療の適応対象になることを⽰しています 。さらに、本研究は、患者さんごとに異 なるSOD1遺伝⼦の変異に応じて最適な治療を選ぶ「個別化医療」の重要性を⽰しています。
まとめ
本研究では、SOD1関連ALSの⽇本⼈1家系において、世界的に稀少な新しいSOD1遺伝⼦変異(インフレーム重複変異)を同定し、予測 されるSOD1タンパク質構造変化および病態機序を明らかにしました。今回の成果は、SOD1関連ALSの発症メカニズムの理解を深めると ともに、ALSの個別化治療や将来的な遺伝⼦治療の発展に貢献することが期待されます。
⽤語解説
筋萎縮性側索硬化症(ALS):
ALSは、体を動かす指令を出す神経(運動ニューロン)が徐々に障害されることで、⼿⾜やのど、呼吸に
関わる筋⾁が次第にやせて弱くなっていく進⾏性の病気です。ALSの多くは遺伝とは関係なく発症しますが、全体の約5〜10%は遺伝⼦
の変化(変異)が原因で起こり、「家族性ALS」と呼ばれます。⽇本⼈では、SOD1遺伝⼦の変異によって⽣じる「SOD1関連ALS」が家
族性ALSの中で最も多く、約40%を占めています1) 。SOD1関連ALSの多くは、常染⾊体顕性(優性)遺伝形式をとります。これは、両親
のうちどちらか⼀⽅から病気の原因となる遺伝⼦変異を受け継ぐことで発症するタイプです。
SOD1:
スーパーオキシドジスムターゼ1(SOD1)は、体内で発⽣する活性酸素の⼀種「スーパーオキシド」を過酸化⽔素へ変換する酵
素であり、細胞を酸化ストレスから守る働きをもつ抗酸化酵素です。また、SOD1遺伝⼦の変異は、家族性ALSの原因の⼀つとされてい
ます。
野⽣型と変異型
野⽣型:多くの⼈に共通してみられる標準的遺伝⼦配列を持ち、研究における⽐較の基準となる遺伝⼦やタンパク質の状態を指します。
変異型:遺伝⼦配列に変化(変異)が⽣じた状態を指します。変異の種類によっては、作られるタンパク質の構造や機能が変化すること
があります。
ミスフォールディング:
タンパク質は体の中で働くために、正しい⽴体構造に折りたたまれる必要があります。しかし、タンパク質の構
造に変化が⽣じると、正しく折りたためず、異常な形になることがあります。これを「ミスフォールディング」と呼びます。
アンチセンス核酸治療:
特定の遺伝⼦の情報をもとに作られるタンパク質の量を減らす治療法です。ALSの治療では、SOD1タンパク質
の量を減らす薬「トフェルセン」が使われています。
参考⽂献
1) Hiroya Naruse et al., Molecular epidemiological study of familial amyotrophic lateral sclerosis in Japanese population by wholeexome sequencing and identification of novel HNRNPA1 mutation, Neurobiology of Aging, Volume 61, 2018, Pages 255.e9-255.e16 https://doi.org/10.1016/j.neurobiolaging.2017.08.030
掲載論文
| 発表雑誌: | Amyotrophic Lateral Sclerosis and Frontotemporal Degeneration 2025 Dec 3:1-11. |
| 論文タイトル: | Novel in-frame duplication variant of SOD1 in a Japanese family with familial amyotrophic lateral sclerosis |
| 筆 者: | Masanori Nakajima*, Hiroya Naruse*, Yuichi Riku, Kunihiro Ueda, Takashi Matsukawa, Jun Mitsui, Yoshitsugu Nakamura, Shimon Ishida, Takashi Yamada, Naoki Moro, Naoki Kotsuki, Kentaro Nagai, Shin-ichi Tokushige, Ayumi Uchibori, Chizuko Oishi, Hiroyuki Yabata, Makoto Urushitani, Yasushi Iwasaki, Hiroyuki Ishiura, Tatsushi Toda, Shoji Tsuji, Yaeko Ichikawa *These authors contributed equally to this work. (中島 昌典1, 成瀬 紘也2, 陸 雄⼀3, 上⽥ 洲裕2, 松川 敬志2, 三井 純2,4, 中村 善胤5, ⽯⽥ 志門5, ⼭⽥ 隆司6, 茂呂 直紀1, 上⽉ 直樹1, 永井 健太郎1, 徳重 真⼀1, 内堀 歩1, ⼤⽯ 知瑞⼦1, ⽮端 博⾏7, 漆⾕ 真7, 岩崎 靖3, ⽯浦 浩之2,8, ⼾⽥ 達史2,9, 辻 省次2,10, 市川 弥⽣⼦1(1脳神経内科学, 2東京⼤学⼤学院医学系研究科神経内科学, 3愛知医科⼤学加齢医科学研究所神経病理部門, 4東京⼤学⼤学院医学系研究科プレシ ジョンメディシン神経学, 5⼤阪医科薬科⼤学脳神経内科, 6⼤阪医科薬科⼤学病理学, 7滋賀医科⼤学脳神経内科学, 8岡⼭⼤学⼤学院医⻭ 薬学総合研究科脳神経内科学, 9国⽴精神・神経医療研究センター病院, 10 国際医療福祉⼤学ゲノム医学研究所)) |
| DOI: | 10.1080/21678421.2025.2593302 |
問い合わせ先
杏林学園広報室 広報室へのお問い合わせはこちらまで




![学納金サイト [在学生・保護者専用]](/assets/images/BlkFeatured_item_tuition.jpg)
